Agenția Europeană a Medicamentului a autorizat imunizarea cu serul Moderna a copiilor cu vârste între 12 și 17 ani
23 Jul, 2021 17:36
1033
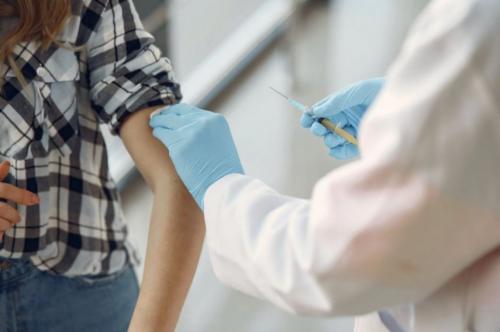
 Agenția Europeană a Medicamentului a aprobat utilizarea serului Moderna pentru imunizarea anti-Covid 19 la copii cu vârsta cuprinsă între 12 și 17 ani.
Agenția Europeană a Medicamentului a aprobat utilizarea serului Moderna pentru imunizarea anti-Covid 19 la copii cu vârsta cuprinsă între 12 și 17 ani.Potrivit unui comunicat al Agenției Europene a Medicamentului comitetul pentru medicamente umane (CHMP) al EMA a recomandat acordarea unei extinderi a indicației pentru vaccinul COVID-19 Spikevax (anterior COVID-19 Vaccine Moderna) pentru a include utilizarea la copii cu vârsta cuprinsă între 12 și 17 ani. Vaccinul este deja autorizat pentru utilizare la persoanele cu vârsta peste 18 ani.
„Utilizarea vaccinului Spikevax la copii cu vârsta cuprinsă între 12 și 17 ani va fi aceeași ca la persoanele cu vârsta de 18 ani și peste. Se administrează sub formă de două injecții în mușchii brațului superior, la distanță de patru săptămâni.
Efectele Spikevax au fost investigate într-un studiu care a implicat 3.732 de copii cu vârste cuprinse între 12 și 17 ani. Acest studiu în curs se desfășoară în conformitate cu planul de investigație pediatrică (PIP) al Spikevax, care a fost agreat de Comitetul pediatric (PDCO) al EMA.
Studiul a arătat că Spikevax a produs un răspuns anticorp comparabil la tinerii cu vârsta cuprinsă între 12 și 17 ani la cel observat la adulții tineri cu vârsta cuprinsă între 18 și 25 de ani (măsurat prin nivelul anticorpilor împotriva SARS-CoV-2). În plus, niciunul dintre 2.163 de copii care au primit vaccinul nu a dezvoltat COVID-19, comparativ cu patru din 1.073 de copii cărora li s-a administrat o injecție falsă. Aceste rezultate au permis CHMP să concluzioneze că eficacitatea Spikevax la copiii cu vârsta cuprinsă între 12 și 17 ani este similară cu cea la adulți“ – se arată în comunicatul citat.
Potrivit aceluiași document cele mai frecvente efecte secundare la copiii cu vârste cuprinse între 12 și 17 ani sunt similare cu cele la persoanele cu vârsta de 18 ani și peste. Acestea includ durere și umflături la locul injectării, oboseală, cefalee, dureri musculare și articulare, ganglioni limfatici măriti, frisoane, greață, vărsături și febră. Aceste efecte sunt de obicei ușoare sau moderate și se îmbunătățesc în câteva zile de la vaccinare.
„CHMP a remarcat faptul că, din cauza numărului limitat de copii și adolescenți incluși în studiu, studiul nu ar fi putut detecta noi reacții adverse mai puțin frecvente sau a estimat riscul de efecte secundare cunoscute, cum ar fi miocardita (inflamația mușchiului inimii) și pericardita (inflamația a membranei din jurul inimii).
Cu toate acestea, profilul general de siguranță al Spikevax determinat la adulți a fost confirmat în studiul la adolescenți; prin urmare, CHMP a considerat că beneficiile Spikevax la copiii cu vârsta cuprinsă între 12 și 17 ani depășesc riscurile, în special la cei cu afecțiuni care cresc riscul de COVID-19 sever.
Siguranța și eficacitatea vaccinului atât la copii, cât și la adulți vor continua să fie monitorizate îndeaproape, deoarece este utilizat în campaniile de vaccinare din toate statele membre, prin intermediul sistemului de farmacovigilență al UE și a studiilor în curs și suplimentare efectuate de companie și de autoritățile europene“ – a mai transmis Agenția Europeană a Medicamentului.
Ti-a placut articolul?
Articole asemanatoare
Mai multe persoane condamnate într-un dosar penal privind vaccinări fictive anti-Covid. Incredibil ce au stabilit anchetatorii
15 Apr 2024 526
MApN prin UM 02464 București achiziționează vaccin împotriva febrei galbene. Doze vor ajunge și la Spitalul Militar de Urgență „Dr. Alexandru Gafencu” din Constanța (DOCUMENT)
25 Feb 2024 752
Compania Pfizer - BioNTech a acționat România în judecată pentru plata tuturor vaccinurilor anti-Covid. Ce a decis Guvernul României
01 Feb 2024 872
Riscul de tulburări menstruale este „uşor crescut" în cele trei luni de la administrarea unui vaccin anticovid
24 Jan 2024 695
Fostul ministru al Sănătății, Vlad Voiculescu, despre dosarul vaccinurilor anti-covid 19 - „Din câte ştiu eu, nu există niciun progres în dosar“
21 Jan 2024 751
Constanța, în topul județelor unde au fost raportate mai multe cazuri de gripă. Un nou deces, la nivel național
04 Jan 2024 1080
Dosarul vaccinărilor presupus false de la Mangalia. Fiul primarului din 23 August a contestat controlul judiciar. Răspunsul instanței (MINUTA)
18 Dec 2023 1191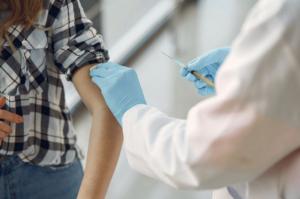
Ioana Mihăilă, urmărită penal în dosarul vaccinurilor anti-Covid 19. Oficial de la DNA despre acuzațiile aduse fostului ministru
08 Dec 2023 754
Fostul ministru, Ioana Mihăilă la DNA „Mi s-a comunicat calitatea de suspect pentru contractul de vaccinuri Pfizer semnat în mai 2021“
08 Dec 2023 676
Fostul ministru al Sănătăţii Ioana Mihăilă, la DNA în dosarul vaccinurilor anti-Covid 19
08 Dec 2023 742
Oficial de la DNA Fostul ministru al Sănătății, Vlad Voiculescu, urmărit penal în dosarul vaccinurilor anti-Covid 19
08 Dec 2023 657

Adauga un comentariu
Nume:
Email:
Comentariu*: